据Apellis制药2月17日宣布,美国食品药品监督管理局(FDA)已批准SYFOVRE(pegcetacoplan)注射剂用于治疗继发于年龄相关性黄斑变性(AMD)的地理萎缩(GA)。该药目前也在欧洲药品管理局接受监管审查,预计2024年初做出决定,此外在加拿大也已提交了新药申请。
眼底病吧 关注:619贴子:2,245
- 4回复贴,共1页
什么是地理萎缩?
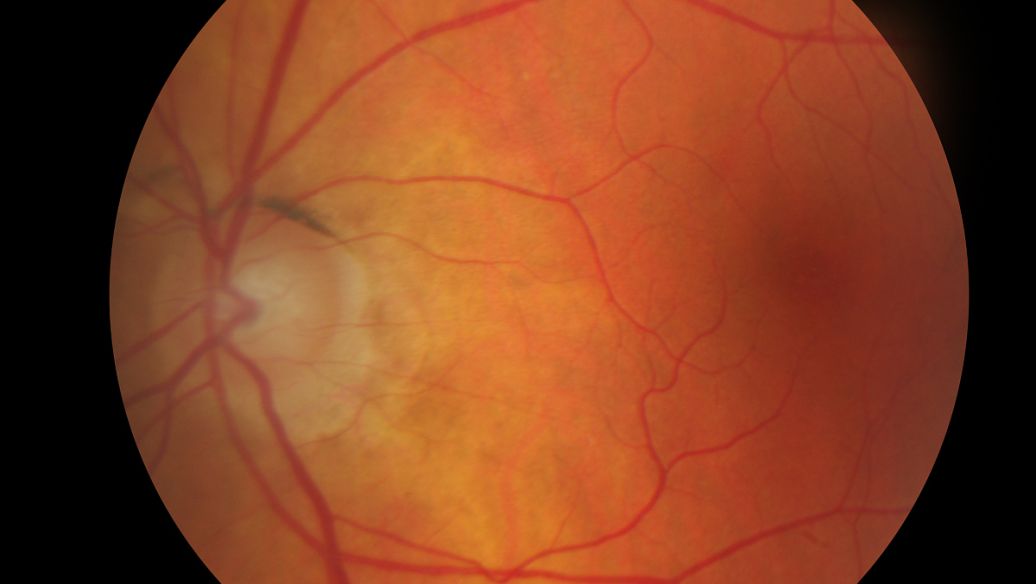
地理萎缩是一种称为年龄相关性黄斑变性(AMD)的退行性视网膜疾病的晚期形式。患有地理萎缩的人会出现破坏视网膜细胞的病变生长,起初会出现中央视力丧失,然后逐渐恶化为完全失明。
虽然针对湿性AMD有几种可以恢复视力的药物,但地理萎缩却没有。这种疾病的进展与补体系统(免疫系统的一部分)的过度活动有关。
地理萎缩是一种称为年龄相关性黄斑变性(AMD)的退行性视网膜疾病的晚期形式。患有地理萎缩的人会出现破坏视网膜细胞的病变生长,起初会出现中央视力丧失,然后逐渐恶化为完全失明。
虽然针对湿性AMD有几种可以恢复视力的药物,但地理萎缩却没有。这种疾病的进展与补体系统(免疫系统的一部分)的过度活动有关。
地理萎缩第一种治疗方法
SYFOVRE是首个FDA批准用于治疗地理萎缩的方法。该药物由两种肽组成,它们共同阻断称为C3的补体系统蛋白,进而全面控制补体级联,补体级联是人体免疫系统的一部分。
这种作用机制也被用于Apellis的第一个FDA批准的药物Empaveli。这种输注疗法可治疗罕见的血液病阵发性睡眠性血红蛋白尿症。
不过需要注意的是,在临床试验中,Syfovre虽然减缓了疾病进展标志物的生长,但未减缓患者视力的退化。
在支持其新药申请的两项关键研究中,有一项没有达到主要目标,这迫使Apellis要求FDA推迟审查以纳入更多数据。因为这种药物不能恢复失去的视力,而治疗其他类型的与年龄相关的视力丧失的药物可以,所以患者可能不容易看到治疗的效果。
SYFOVRE是首个FDA批准用于治疗地理萎缩的方法。该药物由两种肽组成,它们共同阻断称为C3的补体系统蛋白,进而全面控制补体级联,补体级联是人体免疫系统的一部分。
这种作用机制也被用于Apellis的第一个FDA批准的药物Empaveli。这种输注疗法可治疗罕见的血液病阵发性睡眠性血红蛋白尿症。
不过需要注意的是,在临床试验中,Syfovre虽然减缓了疾病进展标志物的生长,但未减缓患者视力的退化。
在支持其新药申请的两项关键研究中,有一项没有达到主要目标,这迫使Apellis要求FDA推迟审查以纳入更多数据。因为这种药物不能恢复失去的视力,而治疗其他类型的与年龄相关的视力丧失的药物可以,所以患者可能不容易看到治疗的效果。
SYFOVRE的疗效及安全性
FDA对SYFOVRE的批准是基于两项假对照3期研究的结果,每项研究都有每月一次给药和每隔一个月一次给药的队列。使用pegcetacoplan治疗实现在24个月时测量的病变生长速度降低,这在两项关键研究中具有可比性。
这两项研究的患者还参与了一项扩展研究,该研究将对他们进行为期3年的跟踪观察,以观察在24个月时观察到的效果是否会持续。在接受每月一次pegcetacoplan给药的队列中,在第18至24个月测量的病变生长最大减少量为36%。
在这两项关键研究中,报告的最常见不良反应是眼部不适、新生血管性年龄相关性黄斑变性(AMD的“湿性”形式)、玻璃体飞蚊症和结膜出血。药物标签警告中称,眼部注射可能导致一种称为眼内炎和视网膜脱离的炎症,不过在临床试验中,不到1%的患者报告了这些问题。
FDA对SYFOVRE的批准是基于两项假对照3期研究的结果,每项研究都有每月一次给药和每隔一个月一次给药的队列。使用pegcetacoplan治疗实现在24个月时测量的病变生长速度降低,这在两项关键研究中具有可比性。
这两项研究的患者还参与了一项扩展研究,该研究将对他们进行为期3年的跟踪观察,以观察在24个月时观察到的效果是否会持续。在接受每月一次pegcetacoplan给药的队列中,在第18至24个月测量的病变生长最大减少量为36%。
在这两项关键研究中,报告的最常见不良反应是眼部不适、新生血管性年龄相关性黄斑变性(AMD的“湿性”形式)、玻璃体飞蚊症和结膜出血。药物标签警告中称,眼部注射可能导致一种称为眼内炎和视网膜脱离的炎症,不过在临床试验中,不到1%的患者报告了这些问题。
地理萎缩其他在研新药
在SYFOVRE获批的同时,IvericBio公司于近日宣布,FDA已接受avacincaptad pegol的申请,这是一种设计用于阻断补体系统蛋白C5的药物。预计8月份将对该药物做出监管决定。
另外,Ionis公司正在开发一种反义寡核苷酸,旨在阻断补体因子b蛋白的产生。
在SYFOVRE获批的同时,IvericBio公司于近日宣布,FDA已接受avacincaptad pegol的申请,这是一种设计用于阻断补体系统蛋白C5的药物。预计8月份将对该药物做出监管决定。
另外,Ionis公司正在开发一种反义寡核苷酸,旨在阻断补体因子b蛋白的产生。
扫二维码下载贴吧客户端
下载贴吧APP
看高清直播、视频!
看高清直播、视频!
贴吧热议榜
- 1S14总决赛参赛队伍出炉2558220
- 2吧友采访杨奇黑口罩本体2075501
- 3KPL年总大名单公布1915004
- 4如何评价叶县强拆果园一事1472931
- 5华为三折叠秒售罄1279954
- 6战神诸神黄昏Steam褒贬不一1158475
- 7《赛博朋克》新动画官宣1008624
- 8iPhone16 Pro测评886811
- 9将逐步恢复日本进口水产品723118
- 10海贼王1127话全图公布564627